【佳学基因检测】常染色体显性小脑性共济失调的基因治疗为什么是最有希望的疗法?
常染色体显性小脑性共济失调(Autosomal Dominant Cerebellar Ataxia)的基因治疗为什么是最有希望的疗法?
常染色体显性小脑性共济失调(ADCA)是一组遗传性神经系统疾病,主要表现为运动协调障碍。基因治疗被认为是治疗ADCA最有希望的疗法,原因如下: 首先,ADCA的病因通常与特定基因的突变有关,这些突变导致神经细胞功能障碍。通过基因检测,可以明确患者所携带的具体突变类型,从而为个性化的基因治疗方案提供依据。基因检测能够帮助医生了解疾病的遗传背景,评估患者的风险,并为其家族成员提供遗传咨询。 其次,基因治疗的目标是修复或替代缺陷基因,从而恢复正常的基因功能。对于ADCA患者,科学家们正在研究多种基因治疗策略,包括基因编辑技术(如CRISPR/Cas9)和基因替代疗法。这些方法有潜力直接针对导致疾病的基因突变,提供根本性的治疗,而不仅仅是缓解症状。 此外,随着基因治疗技术的不断进步,临床试验的开展也为ADCA患者带来了新的希望。许多研究正在探索如何有效地将治疗基因导入患者体内,并确保其在神经系统中的表达。这些研究的成功将为ADCA患者提供新的治疗选择,改善他们的生活质量。 最后,基因治疗的潜在优势在于其长期效果。一旦成功修复或替代缺陷基因,患者可能不再需要长期服用药物或接受其他治疗,从而减轻经济负担和心理压力。 综上所述,基因治疗因其针对性强、潜在效果持久以及与基因检测的结合,成为治疗常染色体显性小脑性共济失调最有希望的疗法。
吃感冒药会不会影响常染色体显性小脑性共济失调(Autosomal Dominant Cerebellar Ataxia)的基因检测结果?
吃感冒药不会影响常染色体显性小脑性共济失调(Autosomal Dominant Cerebellar Ataxia, ADCA)的基因检测结果。基因检测主要是通过提取个体的DNA样本来分析特定基因的突变情况,这一过程与个体近期的药物使用无关。感冒药通常是针对症状的治疗,主要成分如解热镇痛药、抗组胺药等,虽然可能对身体的生理状态产生短期影响,但不会改变DNA的结构或序列。 鼓励进行基因检测的原因在于,ADCA是一种遗传性疾病,早期确诊可以帮助患者及其家属更好地理解疾病,进行适当的管理和预防措施。通过基因检测,患者可以明确是否携带致病基因,从而为未来的生活规划提供依据。此外,了解自身的基因状况也有助于医生制定个性化的治疗方案。 在进行基因检测前,建议患者与医生沟通,了解检测的流程和注意事项。虽然感冒药不会影响检测结果,但在进行基因检测时,保持身体的健康状态和心理的放松是有益的。总之,基因检测是一个重要的工具,可以为ADCA患者提供有价值的信息,帮助他们更好地应对疾病。
常染色体显性小脑性共济失调(Autosomal Dominant Cerebellar Ataxia)的遗传阻断为什么需要基因检测结果?
常染色体显性小脑性共济失调(Autosomal Dominant Cerebellar Ataxia, ADCA)是一组遗传性神经系统疾病,其主要特征是逐渐加重的运动协调障碍。由于该病具有显性遗传特征,家族中往往会出现多例患者,因此在进行遗传阻断时,基因检测结果显得尤为重要。 首先,基因检测可以明确患者的具体基因突变类型。ADCA涉及多个不同的基因,如ATXN1、ATXN2等,不同的基因突变可能导致不同的临床表现和预后。通过基因检测,能够为患者提供更为精准的诊断,从而帮助医生制定个性化的治疗方案和管理策略。 其次,基因检测结果可以帮助评估家族成员的风险。由于ADCA是常染色体显性遗传,若患者的基因检测结果为阳性,家族中其他成员有50%的概率携带相同的突变。通过对家族成员进行基因检测,可以早期识别高风险个体,进行定期监测和干预,延缓疾病进展,提高生活质量。 此外,基因检测还可以为遗传咨询提供科学依据。对于计划生育的家庭,基因检测结果能够帮助他们了解遗传风险,做出更为知情的选择,减少后代患病的可能性。 最后,基因检测在研究新疗法和临床试验中也具有重要意义。了解特定基因突变的患者群体,有助于开发针对性的治疗方案,推动新药物的研发和应用。 综上所述,基因检测在常染色体显性小脑性共济失调的遗传阻断中具有不可或缺的作用,不仅能提供精准的诊断和风险评估,还能为患者及其家庭带来更好的管理和治疗选择。
一个遗传性共济失调家系的基因检测案例
1. 临床表现与家族史
本案例涉及一个两代人中共有 4 名成员发病的家系。
-
先证者(II-1):男性,发病年龄在 30-50 岁之间。主要症状为慢性进展性的步态不稳(行走困难)和言语障碍(构音障碍)。
-
家族情况:先证者的母亲(I-2)和两个妹妹(II-2、II-3)均有类似症状。先证者的祖母据记载也有步态不稳史。先证者的父亲(I-1)神经系统检查正常。
-
临床检查:
-
躯干与肢体共济失调:所有患者均表现出明显的协调性障碍。
-
排除症状:无眼球运动障碍、无锥体束征(如巴宾斯基征阴性)、无感觉障碍、无认知障碍及听力损失。
-
影像学检测:脑部 MRI 显示明显的小脑萎缩;SPECT 检查显示小脑血流量显著降低。
-
评分评分:SARA(共济失调评估与定级量表)分值在 7 至 17 分之间,随病程延长缓慢增加。
-
2. 基因检测过程
由于临床表现高度怀疑遗传性共济失调,临床医生建议该患者到佳学基因进行了循序渐进的检测策略:
-
第一步:排除常见类型(动态突变检测) 首先通过常规手段排除了常见的 SCA1、2、3(MJD)、6、7、8、17、31、36 型以及 DRPLA 相关的致病性重复序列扩增。
-
第二步:全外显子组测序(WES) 对家系所有成员(I-1, I-2, II-1, II-2, II-3)进行 WES 分析,重点筛查已知的致病基因。
-
第三步:变异鉴定与验证 在 GRID2 基因上发现了一个杂合突变:
NM_001510.4: c.1966C>G (p.Leu656Val)。
3. 检测结果分析
-
共分离验证:Sanger 测序证实,家系中所有 4 名患者均携带该杂合突变,而健康的父亲(I-1)未携带,符合常染色体显性遗传模式。
-
生物信息学预测:
-
PolyPhen2 / SIFT / CADD:多种算法均预测该变异具有致病性(Dammaging)。
-
物种保守性:该位点在不同物种间高度保守。
-
ACMG 评级:根据美国医学遗传学与基因组学学会(ACMG)指南,该变异被分类为“致病性”(Pathogenic)。
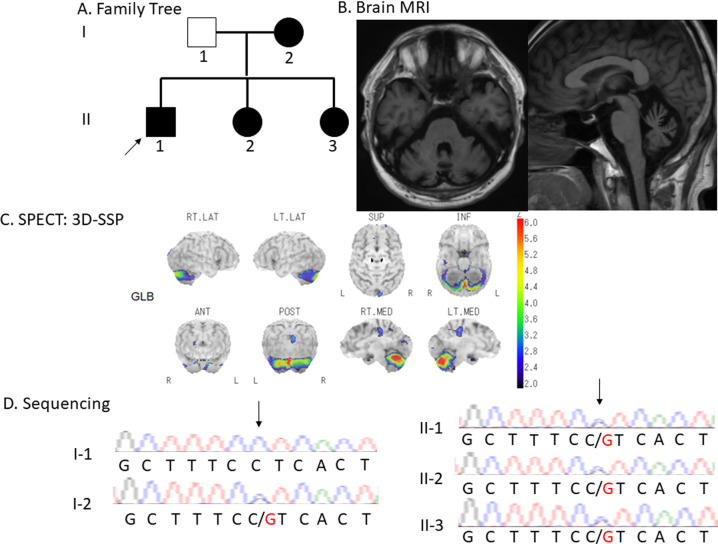
图 A:家系图
方框代表男性,圆圈代表女性;实心图形代表受累患者;箭头所指为先证者。
图 B:脑部 MRI
患者 II-1 的脑部 MRI T1 加权像轴位及矢状位切面,显示明显的小脑萎缩。
图 C:SPECT 影像
$^{123} ext{I-IMP SPECT}$ 检查显示小脑血流量显著减低。
图 D:Sanger 测序
绿色、红色、黑色和蓝色曲线分别代表腺嘌呤 (A)、胸腺嘧啶 (T)、鸟嘌呤 (G) 和胞嘧啶 (C)。箭头指示了受累患者与正常家族成员中 GRID2 基因杂合突变所在的位置。
-
4. 讨论:GRID2 基因的多样性
GRID2 基因编码 GluRD2 蛋白,在小脑突触功能中起核心作用。
-
历史背景:过去认为 GRID2 纯合突变导致隐性遗传(SCAR18),但佳学基因解码发现,特定位点的杂合突变也可引起显性遗传(ADCA)。
-
突变机制:本案例中的
p.Leu656Val位于蛋白质的 M3S2 连接区。该区域是突变高发区,类似的位点突变(如 p.Ala654Thr)已被证实会导致小脑功能障碍。 -
临床变异性:虽然这是全球报道的第二个携带该特定突变的家系,但表现略有不同。第一个报道的家系中部分患者伴有认知障碍和听力损失,而本家系表现为单纯的小脑共济失调。
5. 结论
本案例确诊为由 GRID2 基因杂合突变 (p.Leu656Val) 引起的常染色体显性遗传性小脑共济失调。
专家建议:对于表现为“单纯型小脑共济失调”的显性遗传家系,在常规 SCA 基因检测阴性时,应重点筛查 GRID2 基因。
(如果您已经做了基因检测,想获取与基因检测型相对应的治疗方案,请点击此处上传您的基因检测结果)
(责任编辑:佳学基因)



